Влажный кашель при ОРВИ у детей – что делать?
При наличии характерных симптомов ОРВИ у ребенка (повышение температуры тела, головная боль, першения, покраснения горла, заложенность носа, насморк) специфическое лечение продуктивного кашля не проводится. Нормально функционирующая иммунная система способна самостоятельно справиться с этим симптомом по мере выздоровления. Чтобы помочь ей и ускорить процесс, необходимо соблюдать следующие правила:
- в комнате ребенка следует поддерживать оптимальную температуру (18–20 °С) и влажность (50–60 %). Рекомендуется регулярно проветривать помещение, 2–3 раза в день проводить влажную уборку, отказаться от использования обогревателей и при необходимости использовать бытовые увлажнители воздуха;
- обязательное условие, необходимое, чтобы вылечить сильный влажный кашель у ребенка, – обильное теплое питье (минеральная вода без газа, витаминные морсы, травяные чаи, молоко с медом и т. п.). Строгое соблюдение этой рекомендации облегчает отхождение мокроты, а вместе с ней – токсических продуктов жизнедеятельности вируса;
- если причиной кашля является слизистый назальный секрет, стекающий по задней стенке носоглотки, то для его нормального отхождения на ночь и по утрам специалисты рекомендуют промывать ребенку нос солевым раствором или орошать стенки носовой полости специальным назальным спреем для детей. Состояние облегчит приподнятая повыше подушка;
- соблюдение строгого постельного режима в период лечения ОРВИ не обязательно (умеренная двигательная активность способна существенно облегчить отхождение мокроты);
- в качестве наружного средства при простуде у детей можно использовать мазь Доктор МОМ® Фито. Это препарат содержит в своем составе эфирные масла 4-х лекарственных растений.
При нормальной температуре тела в дополнение к вышеперечисленным методикам ребенку для облечения отхаркивания разрешается делать легкий перкуссионный массаж (аккуратное постукивание кончиками пальцев по спинке в области легких).Чтобы быстрее вылечить влажный кашель у ребенка, не следует забывать о том, как полезны прогулки на улице (естественно, если у него нет высокой температуры). Свежий воздух, поступая в легкие, способствует более глубокому дыханию, стимулирует разжижение и отхождение скопившейся слизи. Усиление продуктивного кашля во время прогулки – вполне нормальное явление, обусловленное усилением кровоснабжения слизистой оболочки бронхов и активизацией работы секреторных желез.
Муколитическая терапия у детей
Е.В. БОЙЦОВА
, д.м.н.,
зав. лабораторией детской пульмонологии НИИ пульмонологии СПбГМУ им. акад. И.П. ПавловаВоспалительные заболевания органов дыхания у детей составляют большую часть обращений за медицинской помощью и представляют важную проблему педиатрии и детской пульмонологии. Ежегодно дети переносят от 5 до 12 эпизодов вирусной инфекции, сопровождающихся поражением нижних и верхних дыхательных путей.
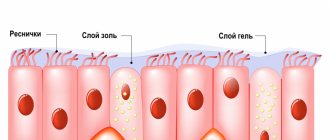
В норме воздух поступает в легкие, проходя через верхние (рото-носоглотка, гортань) и нижние (трахея, бронхи, бронхиолы) дыхательные пути, за это время воздушная струя согревается, увлажняется и очищается. Различные частицы, поступающие в дыхательные пути вместе с воздухом, осаждаются на слизистой и затем выводятся вместе с бронхиальным секретом благодаря системе самоочищения бронхов или мукоцилиарному клиренсу. Мукоцилиарный клиренс осуществляется движением ресничек мерцательного эпителия, обеспечивающих продвижение бронхиального секрета, который секретируется бокаловидными клетками и слизистыми железами. Слизистые железы, отвечающие за продукцию слизи в бронхиальном дереве, появляются в трахее у плода в возрасте 10 недель, постепенно распространяются по направлению к периферии и располагаются как у взрослых уже в кананикулярной стадии (17–27 недель) антенатального развития. В то же время их структурное развитие заканчивается к 13– летнему возрасту. При рождении число бокаловидных клеток составляет 10% от нормы, а к 3 месяцам увеличивается в 4 раза. У младенцев секрет подслизистых желез менее вязкий и почти не содержит сиаловой кислоты. В нормальных условиях движения ресничек происходят в более жидкой части бронхиального секрета – в золе. Золь состоит из секрета желез, капиллярного транссудата, межтканевой жидкости и растворенных химических соединений. Вязкость этого слоя соответствует вязкости плазмы, что обеспечивает эффективные колебания погруженных в золь ресничек [1, 2]. Наружный гель-слой состоит из гликопротеидов, секретируемых бокаловидными клетками, кроме этого, содержит лизоцим, альбумин, альфа-1-антитрипсин, иммуноглобулины А, комплекс липидов, сурфактант, связанные между собой дисульфидными, ионными и другими связями. Вязкость и эластичность бронхиального секрета зависят от количества воды и входящих в его состав гликопротеинов (муцинов). Муцины секрета принадлежат к двум различным типам: 60% гидрофильные кислые сиало и сульфомуцины и нейтральные фукомуцины – гидрофобные. При различных патологических состояниях это соотношение меняется, снижение уровня сиаломуцинов уменьшает водный компонент секрета, что типично для большинства заболеваний органов дыхания. Снижение уровня гидрофильного компонента приводит к увеличению гидрофобных фукомуцинов, что делает бронхиальный секрет более вязким и густым. Бронхиальный секрет слизистого характера вырабатывается бокаловидными клетками, подслизистые железы продуцируют более жидкий серозно-слизистый секрет. Наибольшее количество бокаловидных клеток концентрируется в трахее, по мере продвижения в дистальном направлении количество этих клеток уменьшается и в бронхиолах они отсутствуют. В дистальных отделах дыхательных путей имеются клетки Клара, которые синтезируют фосфолипиды и сурфактант, предполагается, что именно они могут превращаться в бокаловидные клетки при воспалении. Преобладающая активность серозных желез приводит к образованию секрета с низким содержанием гликопротеинов. И наоборот, гиперплазия бокаловидных клеток с распространением в периферические отделы бронхиального дерева, что наблюдается при острых и хронических бронхиолитах, бронхиальной астме и других заболеваниях дыхательных путей у детей, характеризуется повышением содержания гликопротеинов, фракции геля и увеличением вязкости бронхиального секрета [2]. При воспалении в дыхательных путях значительно увеличивается содержание продуктов распада микроорганизмов, экссудата (вода, белки, ионы), что также повышает вязкость. Скопление вязкого бронхиального секрета может привести к вентиляционным нарушениям и к снижению местной иммунологической защиты дыхательных путей, что способствует колонизации патогенной микрофлорой с высоким риском развития затяжного и хронического воспалительного процесса [3, 4]. С другой стороны, бактериальные ферменты и лизосомальные протеазы могут изменять сиаломуцины и приводить к утрате способности формировать волокнистые структуры, что делает секрет излишне жидким и неэластичным, что также снижает эффективность мукоцилиарного очищения респираторного тракта [1, 4]. Все это делает актуальным использование лекарственных средств, воздействующих на секреторную активность слизистой или на секрет при помощи различных механизмов.
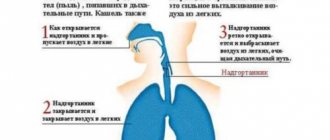
При снижении эффективности системы очищения появляется кашель. Кашель – нормальная реакция организма на раздражение, сложный механизм, способствующий очищению дыхательных путей. В то же время кашель является симптомом большого числа различных заболеваний. Выделяется более 50 причин кашля, возникновение этого симптома требует проведения широкого диагностического поиска. Чаще всего кашель связан с патологией верхних и нижних дыхательных путей, кашель полезен, и терапевтической задачей является повышение его эффективности. Подавление кашля требуется лишь в тех случаях, когда он не несет функции очищения бронхов, например при коклюше, навязчивом сухом или психогенном кашле [4, 5]. В этом случае используются противокашлевые средства центрального наркотического и ненаркотического действия. Противокашлевые препараты наркотического действия понижают чувствительность дыхательного центра, подавляют функцию ресничек и могут вызвать судороги. В педиатрической практике используются ненаркотические препараты центрального действия, которые могут назначаться детям с первых месяцев жизни.
При влажном продуктивном кашле, бронхиальной обструкции противокашлевые препараты центрального действия противопоказаны. Имеется ряд препаратов с опосредованным противокашлевым действием. Назначение бронхолитиков способствует ликвидации бронхоспазма и облегчению спазматического кашля. Препараты с противовоспалительным эффектом, например фенспирид или ингаляционные стероиды, также могут облегчать кашель за счет уменьшения воспалительных изменений слизистой оболочки и снижения патологической импульсации [5]. Использование антигистаминных средств для лечения кашля нецелесообразно, т. к. они сгущают мокроту и ухудшают ее дренаж.
В настоящее время существует множество препаратов, воздействующих на мокроту и применяющихся при различных острых и хронических заболеваниях дыхательных путей. Известны традиционные отхаркивающие средства, влияющие на золь-слой мокроты. Это препараты рефлекторного действия, увлажняющие средства и стимуляторы бронхиальных желез. К препаратам рефлекторного действия относятся растительные экстракты. Они раздражают слизистую желудка, возбуждают рвотный центр и усиливают перистальтику бронхов, рефлекторно стимулируют секрецию слюнных и слизистых желез бронхов, что увеличивает количество мокроты и, как следствие, облегчает кашель. Большинство этих препаратов содержат эфирные масла, которые выделяются через дыхательные пути и усиливают секрецию в малых дозах, а в более высокой концентрации вызывают сужение кровеносных сосудов и уменьшение секреции. Препараты с осторожностью назначаются в раннем возрасте, особенно у детей с поражением ЦНС, т. к. усиление рвотного рефлекса может стать причиной аспирации и асфиксии. Не показаны они у детей с аллергией на травы. К отхаркивающим средствам резорбтивного действия (стимуляторам бронхиальных желез) относятся солевые препараты (иодиды калия, натрия, аммония хлорид). Считается, что использование этих препаратов в педиатрии должно быть ограничено, т. к. отхаркивающий эффект йодидов наблюдается в высоких дозах и они имеют неприятный вкус [5]. К отрицательным свойствам противокашлевых средств относят и необходимость их частого применения (каждые 2–4 часа) [6]. Комбинация отхаркивающих и противокашлевых согласно исследованиям у взрослых ухудшают показатели функции внешнего дыхания [7].
Определенный эффект оказывают увлажняющие средства, к которым относятся обильное питье, водные и паровые ингаляции. В последнее время активно изучаются муколитические свойства гипертонического раствора NaCL. Основной механизм действия раствора – регидратация бронхолегочного секрета, что приводит к улучшению мукоцилиарного клиренса. Большинство исследований посвящено изучению роли гипертонического раствора в терапии муковисцидоза. Было достоверно показано, что гипертонический раствор хорошо переносится (именно 7%, более высокие концентрации вызывают обструкцию, низкие – менее эффективны), улучшает функцию легких, снижает количество обострений бронхолегочного процесса, улучшает качество жизни пациентов [8, 9]. Гипертонический раствор поваренной соли используется при лечении острых бронхиолитов у детей раннего возраста. Несмотря на противоречивость литературных данных, преобладает мнение, что 3% раствор NaCL с бета-2-агонистами или адреналином улучшает клиническое течение болезни и сокращает ее длительность [7].
Эффективность отхаркивающих средств при остром и хроническом поражении дыхательных путей значительно уступает современным мукоактивным препаратам [6, 7]. Мукоактивные препараты изменяют свойства гель–слоя мокроты. Среди них выделяют препараты прямого муколитического действия, включающие тиолитики и протеолитические ферменты и непрямого действия – секретолитики и мукорегуляторы.
Высокоактивными муколитиками являются производные цистеина со свободной тиоловой группой (N-ацетилцистеин). Механизм действия их основан на разрыве дисульфидных связей белков мокроты, при этом снижается полимеризация молекул и мокрота становится менее вязкой. Считается, что N-ацетилцистеин обладает более выраженной, чем у остальных муколитиков, способностью разжижать гнойную мокроту, лизировать фибрин и кровяные сгустки. Известно, что N-ацетилцистеин уменьшает гиперплазию бокаловидных клеток и гиперсекрецию слизи [10, 11]. Показаниями для применения этого средства являются клинические состояния, при которых отмечается кашель с густой, вязкой, трудноотделяемой мокротой (чаще это обострение хронических инфекционно-воспалительных, наследственных и врожденных заболеваний легких) [4, 11]. N-ацетилцистеин важен при лечении больных муковисцидозом. Препарат выпускается в различных формах: в виде шипучих таблеток, раствора для ингаляций и местного применения при бронхоскопии и для введения в пазухи при пункции, для внутримышечного введения. При одновременном назначении с антибиотиками следует соблюдать 2-часовой перерыв между приемом препаратов. Установлено, что N-ацетилцистеин не влияет на биодоступность амоксициллина и доксициклина и незначительно снижает абсорбцию цефалексина. Совместное применение ацетилцистеина с эритромицином значительно повышает абсорбцию последнего [11]. Использование препарата необходимо совмещать с кинезитерапией, т. к. возможно формирование излишне жидкого секрета, что может приводить к еще большему ухудшению мукоцилиарного клиренса, а это особенно нежелательно у детей раннего возраста [1, 2]. Препарат обладает многогранными химическими свойствами, обусловленными его химической структурой. Антиоксидантная активность N-ацетилцистеина прямым взаимодействием тиольной группы и свободных радикалов, с другой стороны, являясь предшественником глютатиона, усиливает активность многих ферментов, участвующих в поддержании баланса в системе оксиданты и антиоксиданты. С антиоксидантной активностью связана способность N-ацетилцистеина предупреждать заболеваемость ОРВИ и повышать противоинфекционный иммунитет, замедлять снижение легочной функции при ХОБЛ у взрослых, снижать темпы прогрессирования легочного фиброза при интерстициальных болезнях [10]. Противовоспалительный эффект N-ацетилцистеина проявляется при длительном применении в высоких дозах и изучен у взрослых пациентов. Установлено, что препарат снижает адгезию бактерий к слизистой оболочке ротоглотки, которая является резервуаром эндобронхиальной инфекции [11]. Возможно, с этим механизмом связана способность N-ацетилцистеина снижать частоту респираторных заболеваний у детей при профилактическом назначении [12]. N-ацетилцистеин для внутримышечного введения в возрасте до 1 года используется только по жизненным показаниям в условиях стационара в связи с риском «затопления», другими побочными эффектами являются диспептические нарушения, аллергические реакции.
Дорназа альфа – генно-инженерный муколитик, препарат, применяемый преимущественно при муковисцидозе в ингаляционной форме, представляющий собой рекомбинантную человеческую ДНазу. Известно, что гнойный секрет в высокой концентрации содержит внеклеточную ДНК, которая является вязким полианионом, высвобождающимся из разрушающихся лейкоцитов, накапливающихся в мокроте в результате бактериальной инфекции. Дорназа альфа вызывает гидролиз внеклеточной ДНК и значительно снижает вязкость секрета. Кроме этого, препарат эффективно влияет на деструктивный компонент воспаления в легочной ткани, уменьшая процент нейтрофилов, понижая концентрацию эластазы, интерлейкина-8 и матричных металлопротеиназ, в бронхиальном содержимом и способствует разрушению биофильма мукоидной синегнойной палочки. Проведенные исследования демонстрируют, что дорназа альфа является эффективным средством для лечения и других хронических заболеваний легких у детей, сопровождающихся бронхореей с вязкой и гнойной мокротой [13]. Побочные эффекты, как правило, незначительны и редки.
К секретолитическим мукоактивным препаратам относят производные алколоида вазицина (бромгексин и амброксол). Их муколитический эффект связан с деполимеризацией мукопротеиновых и мукополисахаридовых волокон [1, 2]. Клиническая эффективность амброксола значительно выше, чем бромгексина [1, 6]. Амброксол стимулирует выработку сурфактанта и замедляет его распад, что улучшает скольжение секрета по эпителию, его текучесть, и повышает мукоцилиарный клиренс. При бактериальной инфекции при одновременном назначении амброксола и антибиотиков отмечено повышение концентрации антибактериальных средств в легочной ткани. Этот эффект описан при терапии амоксициллином, эритромицином, цефуроксимом и доксициклином [3, 14]. Противовоспалительное действие амброксола связывают с подавляющим действием на продукцию мононуклеарами медиаторов воспаления и увеличением макрофагальной активности [15]. При затяжном течении обострения БА у детей назначение противоастматической терапии рекомендуется сочетать с применением амброксола, т. к. кроме улучшения реологических свойств мокроты этот препарат способен подавлять высвобождение гистамина, лекотриенов и провоспалительных цитокинов из тучных клеток [15, 16]. Муколитический эффект амброксола не сопровождается увеличением количества секрета. Амброксол может применяться без возрастных ограничений, выпускается в разных формах: сироп, таблетки, жидкие формы для ингаляций и приема внутрь. Имеются клинические данные, свидетельствующие о повышении эффективности препарата у детей при сочетании различных форм доставки при хронической бронхолегочной патологии и обострении бронхиальной астмы [6]. Побочные эффекты редки и включают аллергические реакции и диспептические нарушения.
Современные мукорегуляторные средства восстанавливают секреторную функцию бокаловидных клеток, нормализуют реологические свойства секрета. В отличие от секретолитических препаратов, местом приложения которых является патологический секрет, мукорегуляторы действуют непосредственно на железистую клетку, регулируя ее секреторную функцию независимо от исходного патологического состояния. К этой группе относятся препараты на основе карбоцистеина. Механизм действия карбоцистеина основан на нормализации соотношения кислых сиаломуцинов и нейтральных фукомуцинов с помощью активации сиаловой трансферазы, ингибирования ферментов, участвующих в переносе углеводных остатков на белковую основу муцинов [2, 3]. Восстановление нормального соотношения кислых и нейтральных муцинов в бронхиальном секрете нормализует вязкость и эластичность мокроты, повышает эффективность мукоцилиарного транспорта и способствует быстрой ликвидации воспаления. Под воздействием карбоцистеина происходит регенерация слизистой оболочки, восстановление ее структуры, нормализация количества бокаловидных клеток, что уменьшает объем секреции. Карбоцистеин значительно снижает оксидативный стресс, предотвращая образование свободных радикалов при воспалительном процессе [4]. Кроме прямого влияния на секретирующие клетки обнаружен эффект карбоцистеина на внутриклеточный транспорт ионов, заключающийся в открытии хлорных каналов и регуляции тока воды, благодаря этому появились дополнительные показания к назначению препарата при муковисцидозе. Установлено, что у больных, получающих терапию препаратами карбоцистеина, повышается концентрация секреторного иммуноглобулина А [17]. Карбоцистеин не эффективен при аэрозольном применении, имеет высокую кислотность, что создает возможность негативного влияния на слизистую оболочку желудка. Соединение карбоцистеина с лизином обеспечивает лучшее всасывание действующего вещества и не раздражает слизистую желудка. Считается, что этот мукорегулятор можно использовать на ранних сроках острых респираторных заболеваний для предотвращения секреторных нарушений. При хронических заболеваниях легких хорошая переносимость позволяет принимать препарат длительно, нормализация свойств секрета сохраняется в течение 8–13 дней после окончания 4-дневного курса приема, что позволяет длительно принимать комбинацию карбоцистеина и лизина повторными курсами с перерывом [3, 19, 18]. Для препаратов группы карбоцистеина характерен синергизм с антибиотиками, при совместном применении отмечается повышенное накопление антибактериального препарата в тканях и секрете респираторного тракта [4]. Действие карбоцистеина на все поврежденные отделы дыхательных путей, в том числе и пазухи носа, а также среднее и внутреннее ухо. Использование карбоцистеина оказалось эффективным в комплексном лечении острого и рецидивирующего и хронического отита у детей в возрасте от 2 до 12 лет [20]. Известно, что главным механизмом эвакуации слизи из синусов и барабанной полости является мукоцилиарный клиренс, т. к. эти структуры находятся в стороне от общего потока воздуха в носоглотке и имеют только узкое сообщение с ней. Назначение карбоцистеина в комбинации с антибиотиками у детей и взрослых с острыми и хроническими риносинуситами продемонстрировало быструю положительную динамику клинических симптомов, что связывают со стимулирующим влиянием препарата на реснитчатый эпителий [21]. Эффект карбоцистеина подтвержден при лечении хронического аденоидита, включение препарата в протокол лечения приводило к более быстрому улучшению по сравнению с традиционной терапией [22]. В экспериментах при заражении in vitro культуры клеток человеческой трахеи риновирусом, вирусом гриппа А, риносинтициальным вирусом препарат ингибировал внедрение его в клетку, снижая мембранную экспрессию вирусных рецепторов [4]. В других экспериментах показано влияние препарата в отношении бактериальных патогенов, применение карбоцистеина предотвращало адгезию St. pneumonia к клеткам дыхательного эпителия также путем уменьшения числа специфических рецепторов [23]. Таким образом, карбоцистеин является препаратом выбора при острой и хронической бронхолегочной патологии, в том числе и при сочетании поражения бронхолегочной системы и ЛОР органов. В последнее время активно изучаются противовирусные свойства карбоцистеина. Препарат может назначаться с возраста 1 месяц, не рекомендуется использовать у детей со склонностью к запорам и при язвенной болезни.
Выбор мукоактивного средства определяется индивидуальными особенностями больного, характером и течением заболевания, особенностями кашля и мокроты. При острой инфекции верхних дыхательных путей, протекающей с сухим кашлем, показаны увлажняющие процедуры, средства с обволакивающим периферическим действием, у старших детей препараты центрального действия. При острых заболеваниях верхних и нижних дыхательных путей и легких в начале заболевания, сопровождающегося сухим кашлем, показаны препараты, стимулирующие секрецию, при продуктивном кашле – мукорегуляторы, нормализующие слизеобразование и состав секрета. Вязкая гнойная мокрота, характерная для больных с хроническими заболеваниями бронхо-легочной системы, требует назначения препаратов, разрушающих полимеры слизи. При поражении дистальных отделов бронхиального дерева, характеризующейся обструкции и сниженной продукции сурфактанта у детей раннего возраста эффективным будет назначение секретолитических препаратов, стимулирующих выработку сурфактанта, не увеличивающих количество мокроты. При сочетанном поражении дыхательных путей и ЛОР органов используются мукорегуляторы, хорошо проникающие в полости носа, внутреннее и среднее ухо.
Литература
1. Мизерницкий Ю.Л. Отхаркивающие и муколитические средства в терапии бронхолегочных заболеваний у детей. // Царегородцев А.Д., Таболин В.А. (ред.) Руководство по фармакотерапии в педиатрии и детской хирургии. М., Медпрактика, 2002. С. 123-140. 2. Синопальников А.И., Клячкина И.Л. Муколитическая терапия при хроническом обструктивном бронхите. // Чучалин А.Г. (ред). Хронические обструктивные заболевания легких. М.; 1998. С. 275-291. 3. Илькович М.М., Гембицкая Т.Е., Панина Н.Т. Фармакологическая коррекция нарушений мукоцилиарного клиренса у больных острыми и хроническими заболеваниями легких. Пульмонология. 2009. №6. С. 101-106. 4. Марушко Ю.В. Применение карбоцистеина в терапии респираторной патологии у детей. Современная педиатрия. 2012. №4 (44). С. 1-6. 5. Г.А. Самсыгина Противокашлевые препараты в педиатрии.Consilium medicum. Приложение. 2001. №2. С. 18-22.
Полный список литературы вы можете запросить в редакции
Что давать ребенку при влажном кашле?
В качестве средств дополнительного лечения влажного детского кашля специалисты в ряде случаев рекомендуют принимать отхаркивающие препараты. Среди большого разнообразия средств от кашля следует выделить сироп Доктор МОМ®, изготовленный на основе растительных экстрактов. Он способен не только очистить бронхи от скопившейся патологической слизи, но и оказать противовоспалительное действие.Обращаем ваше внимание! Прием отхаркивающего средства не отменяет необходимость использования других терапевтических факторов – регулярного проветривания, поддержания оптимальной температуры и влажности воздуха в помещении, обильного теплого питья и т. п. Что касается лечения влажного кашля у ребенка народными средствами, то оно допустимо только после предварительной консультации со специалистом.
Как работают отхаркивающие и муколитические средства
Отхаркивающие препараты – медикаменты, которые очищают дыхательные пути от мокроты. По принципу действия их разделяют на 2 категории:
- Разжижающие слизь (секретолитики) – уменьшают вязкость мокроты. Одни лекарства увеличивают концентрацию легочных ПАВ (сурфактанта), другие разрушают связи в белках слизи.
- Стимулирующие отхаркивание (секретомоторные) – стимулируют продвижение мокроты к горлу. Одни препараты провоцируют кашель, а вторые усиливают выработку жидкой составляющей мокроты.
Отхаркивающее средство от кашля для детей очищает нижние дыхательные пути от бронхиального секрета, что снижает риск вторичных инфекций.
Влажный кашель у ребенка при бронхите
Если у ребенка уже снизилась температура, но все еще наблюдаются апатия, слабость, бледность кожных покровов и болезненные приступы кашля (как продуктивного, так и непродуктивного), возможно, имеет место воспалительный процесс и развитие осложнений (бронхита или воспаления легких). В данной ситуации для подтверждения или опровержения диагноза обязательно требуется помощь специалиста, который назначит необходимые исследования и даст соответствующие рекомендации по лечению.Внимание! Прием антибиотиков должен проводиться только с разрешения и под наблюдением врача. Самостоятельный выбор антибактериальных средств для ребенка, в связи с наличием большого количества противопоказаний, категорически запрещен!
Среди педиатров продолжаются бурные дискуссии по поводу тактики терапии самого частого и яркого симптома у детей при острой респираторной инфекции (ОРИ) – кашля. И если теоретические аспекты этого явления хорошо изучены, многие патогенетические механизмы понятны и тщательно исследованы, то по поводу рационального лечения кашля у детей на фоне вирусных респираторных инфекций порой существуют принципиальные разногласия [1, 2]. Несмотря на то что в Кокрейновских обзорах с позиции доказательной медицины нам предоставлены результаты научных работ, которыми рекомендовано пользоваться врачу, на практике выбор схемы терапии каждый раз вызывает большие трудности и споры, особенно для педиатра. Это вполне объяснимо, т.к. каждый врач обладает большим личным практическим опытом удачных и противоречивых клинических случаев, собственными наблюдениями и мнением коллег. Существующий сегодня список лекарственных средств огромен, это часто приводит к полипрагмазии, к необоснованному назначению препаратов. Однако решение мы должны принимать согласно утвержденным стандартам лечения и федеральным клиническим рекомендациям.
Актуальность проблемы сохраняется и по сей день. Болезни органов дыхания у детей по-прежнему лидируют по частоте, достигая 50–73% в структуре детской заболеваемости. Так, по данным главного внештатного пульмонолога Москвы профессора А.Б. Малахова, общая заболеваемость болезнями органов дыхания среди детей за последние годы остается на высоком уровне и не имеет тенденции к снижению. На 100 тыс. детского населения приходится 50 тыс. случаев ОРИ (табл. 1) [3–6].
К самым частым проявлениям респираторного заболевания относится кашель. С подобной жалобой чаще всего и обращаются к педиатру. Надо ли его «лечить» на фоне ОРИ? Как часто в педиатрии применяются противокашлевые препараты? К препаратам, которые устраняют кашлевой рефлекс, относятся т.н. наркотические противокашлевые препараты на основе кодеина и его производных и группа ненаркотических противокашлевых средств. Активными веществами для средств центрального типа действия являются окселадин цитрат, пентоксиверин, декстрометофан, бутамират цитрат, глауцина гидрохлорид. К активным веществам периферического типа действия относится преноксадиазина гидрохлорид. Применение подобных препаратов в отношении детей может быть небезопасным. При ОРИ, которая сопровождается наличием вязкой мокроты и влажным кашлем, абсолютно недопустимо подавлять кашлевой центр и блокировать кашель как основной защитный механизм очищения дыхательных путей. Эти препараты могут вызывать у детей нежелательные явления в виде повышенной сонливости, угнетения дыхания, запоров и мн. др. Поэтому в данной клинической ситуации они противопоказаны.
В педиатрии существуют довольно строгие показания к назначению противокашлевых препаратов. Это кашель, вызванный установленной причиной инфекции: либо коклюш, либо коревой трахеит. Педиатр может однократно применять противокашлевое средство, если приступообразный мучительный кашель значительно нарушает сон и прием пищи, вызывает рвоту, а самочувствие ребенка катастрофически страдает. Есть и хирургические причины кашля, где действительно требуется срочное его подавление, например в торакальной хирургии или при остром пневмотораксе. Детям с тяжелыми формами патологии центральной нервной системы при возникновении высокого риска аспирации также возможно периодическое назначение препаратов, которые подавляют кашлевой рефлекс [7].
Довольно серьезной и частой врачебной ошибкой остается одновременное назначение муколитических и противокашлевых препаратов. Отсюда и возникает один из мифов о «заболачивании легких». Нельзя, с одной стороны, разжижать мокроту, с другой – одновременно блокировать механизм ее эвакуации [8]. Практика показывает, что отхаркивающие препараты часто применяются при кашле на фоне ОРИ и не только назначаются педиатрами, но и самостоятельно активно покупаются в аптеке родителями. Отхаркивающие, или т.н. секретомоторные, средства должны усиливать откашливание. Они различаются не только по механизму действия, но и по составу активно действующего вещества. Препараты растительного происхождения (алтей, истода, термопсис и другие лекарственные травы), терпингидрат и ликорин, а также эфирные масла обладают слабым разжижающим действием, стимулируют образование слизи в бронхах.
К сожалению, они также воздействуют и на слюнные железы, что является нежелательным эффектом. Препараты на основе различных солей, например натрия йодид, калия йодид и аммония хлорид, способны стимулировать бронхиальную секрецию и слабо разжижать мокроту. Однако педиатру необходимо учитывать, что данная группа препаратов имеет побочные эффекты, существенные для ребенка, например свойство повышать рвотный рефлекс, вызывать различные аллергические реакции, более того, эти препараты существенно увеличивают объем мокроты. Многие средства растительного происхождения имеют многокомпонентный состав, и невозможно предположить, как все эти компоненты будут взаимодействовать [9]. К тому же период действия данных препаратов довольно короток (обычно 2–3 часа), возникает потребность повторного приема, что в целом может приводить к передозировке и определенным осложнениям [10].
Эффективность безрецептурных средств при ОРИ для детей и взрослых была показана в Кокрейновском обзоре за 2014 г. Было проанализировано 29 исследований: 19 (3799 пациентов) –взрослых и 10 (1036 пациентов) – детей [11]. Было показано, что для отхаркивающих препаратов не проводилось исследований, отвечающих требованиям доказательной медицины. При использовании противокашлевых препаратов, которые подавляют кашель, не выявлено преимуществ перед плацебо. И только у группы муколитических препаратов была доказана эффективность по сравнению с плацебо.
Обзор Кокрейновского сотрудничества за 2013 г. по муколитикам (ацетилцистеин и карбоцистеин) при ОРИ у детей в возрасте до 13 лет доказал безопасность их применения на основании 34 (у 2064 пациентов) исследований с использованием клинических, биологических, радиографических параметров и параметров оценки функции внешнего дыхания. Эффективность была оценена в 6 плацебо-контролируемых исследованиях (497 пациентов). Было четко установлено, что препараты эффективны и имеют высокий профиль безопасности для детей старше двух лет. Необходимо отметить, что в клинических исследованиях не было зафиксировано ни одного случая т.н. синдрома заболачивания легких и ни одного случая возникновения бронхоспазма, которых иногда опасаются практикующие педиатры [12].
Современные муколитики созданы на основе различных химических формул, чем и объясняются различные их механизмы действия (табл. 2). Глядя на информацию в таблице, можно определиться, какой муколитик целесообразно применять в конкретной клинической ситуации и выбирать не по названию, а по механизму действия активного вещества.
Ацетилцистеин и амброксол входят в список жизненно необходимых и важных лекарственных препаратов, а дорназа альфа по программе «7 нозологий» – в базисную терапию муковисцидоза. С целью оценки эффективности, переносимости и безопасности муколитиков для детей при ОРИ, было проведено исследование 259 детей с острой и хронической бронхолегочной патологией в возрасте до 15 лет. Дети получали лечение в течение 5–15 дней: 92 ребенка получали ацетилцистеин, 117 – амброксол, 30 – бромгексин и 20 – мукалтин. Авторы показали, что наилучший клинический эффект от детей с острым бронхитом был получен при применении ацетилцистеина. При назначении бромгексина и амброксола также отмечен выраженный муколитический эффект, но в более поздние сроки от начала лечения.
В приступном периоде бронхиальной астмы при назначении ацетилцистеина в комплексной терапии наилучший эффект был достигнут детьми младшей возрастной группы [7, 13]. Помимо муколитического действия у молекулы ацетилцистеина есть и два дополнительных эффекта. Благодаря тройному действию – муколитическому, антиоксидантному и противовоспалительному – применение ацетилцистеина при ОРИ способствует сокращению длительности кашля, уменьшению интенсивности воспалительной реакции и сокращению продолжительности заболевания. Муколитическое действие ацетилцистеина обусловлено наличием в молекуле ацетилцистеина SH-группы, которая разрывает дисульфидные связи кислых мукополисахаридов мокроты, напрямую изменяет реологические свойства мокроты, уменьшает ее вязкость и адгезивность. Прямое антиоксидантное действие молекулы ацетилцистеина объясняется тем, что реактивные SH-группы связываются со свободными радикалами и таким образом нейтрализуют их. А непрямое антиоксидантное действие возникает из-за способности ацетилцистеина влиять на синтез глутатиона. Противовоспалительное действие связано с возможностью данной молекулы повышать защиту клеток от повреждающего действия свободнорадикального окисления, свойственного воспалительной реакции. Практическое значение этого тройного действия для пациентов показано в исследовательской работе, в которой под наблюдением находились 60 детей в возрасте от 2 до 10 лет с клиническими проявлениями острого респираторного заболевания и с трудноотделяемой мокротой (острый бронхит, в т.ч. с обструктивным синдромом, острый стенозирующий ларинготрахеит, пневмония).
В результате наблюдения показано, что использование ацетилцистеина в комплексной терапии острых заболеваний органов дыхания у детей способствует не только более быстрому достижению продуктивного кашля с улучшением дренажной функции бронхов и уменьшению продолжительности кашля, но и более быстрому купированию симптомов интоксикации и лихорадки, что способствовало уменьшению сроков госпитализации детей с острыми респираторными заболеваниями [14].
О безопасности и хорошей переносимости препарата можно судить по тому, как он переносится при хронических состояниях, например при хроническом бронхите, когда терапия проводится длительными курсами. Кокрейновский обзор, проведенный в 2015 г., показал, что в исследованиях с участием 9367 пациентов на фоне применения муколитиков более 10 месяцев отмечено сокращение числа обострений. Безопасными оказались все используемые муколитики (в т.ч. ацетилцистеин, карбоцистеин, амброксол и бромгексин), и все хорошо переносились [15]. Однако в данный обзор были включены исследования взрослых. Что касается детей, то длительное применение муколитиков в течение 12 месяцев было показано в 4 исследованиях с участием 149 детей старше двух лет, страдавших муковисцидозом. Полученные результаты не выявили значимых клинических различий между ацетилцистеином и амброксолом, серьезные побочные эффекты отсутствовали как при ингаляционном, так и при пероральном применении, препараты хорошо переносились [16, 17].
Важный для педиатра практический вопрос: как действуют муколитики при инфекции верхних дыхательных путей? В показаниях к назначению ацетилцистеина и карбоцистеина в отличие от других муколитиков прописано их назначение и при инфекции верхних дыхательных путей, таких как катаральный и гнойный отит, острый и хронический синусит. Это и понятно, поскольку слизистая дыхательных путей начинается с носовой полости и заканчивается глубоко в бронхиолах. Поэтому законы воспаления при инфекции, патогенез развития острого бронхита и острого ринита схожие на всем протяжении респираторного тракта. Свои муколитические и противовоспалительные свойства молекула ацетилцистеина будет проявлять одинаково и в нижних дыхательных путях, и в верхних. Специалисты-оториноларингологи широко используют в своей практике ацетилцистеин [18–20].
В момент острой инфекции на слизистой респираторного тракта возникает воспаление и образуется вязкий секрет, что приводит к блокировке мукоцилиарного транспорта, развивается мукостаз и как следствие – микробная колонизация. ОРИ, как правило, вызываются вирусами, но бактериальные осложнения могут потребовать назначения антибактериальной терапии. Проведенный обзор показал, что все муколитики при необходимости хорошо сочетаются с антибиотиками (табл. 3) [21, 22].
В некоторых работах было показано применительно к молекуле ацетилцистеина, что она увеличивает клиническую эффективность антибактериальной терапии за счет подавления роста и разрушения бактериальных биопленок [23, 24]. Проведено сравнительное исследование эффективности воздействия мукоактивных препаратов на уменьшение жизнестойкости биопленок, производимых штаммами S. aureus [25]. Было установлено, что активность ацетилцистеина превышала в 5,5 раз таковую амброксола и бромгексина.
Комбинация ацетилцистеина с антибиотиками пенициллинового ряда при острых бронхитах и пневмонии способствует снижению интенсивности кашля уже к третьим суткам от начала лечения, а с цефалоспоринами (например, цефуроксимом) повышает эффективность при бактериальных инфекциях дыхательного тракта [26–29].
Каждый раз педиатр должен выбирать не только непосредственно препарат, но и наиболее эффективный путь его введения. На сегодняшний день у ацетилцистеина и амброксола имеются лекарственные формы в виде растворов для небулайзерной терапии в отличие от карбоцистеина. Безусловно это инновационная технология. Но и у небулайзерного метода введения есть свои недостатки. Прежде всего наличие в семье больного ребенка самого прибора – современного и хорошего качества. Психологические особенности ребенка не всегда позволяют проводить процедуру ингаляции. Она занимает достаточно много времени, требует полной физической и эмоциональной отдачи. При данном пути введения лекарства нет системного эффекта. Это можно считать положительным фактом [30]. Но, в случае когда надо оказать воздействие не только на нижние дыхательные пути, но и на верхние, снять симптомы интоксикации, потребуется прием муколитика внутрь. Небулайзерная терапия заслуженно широко используется как в стационарах, так и в амбулаторной практике. Но в большинстве случаев нет никакой необходимости в ингаляционной доставке, т.к. биодоступность лекарственных средств при приеме внутрь достаточная. Необходимо рационально балансировать в принятии решения в зависимости от конкретной клинической ситуации с больным.
В обычной практике нецелесообразно назначать несколько муколитиков одновременно. Нет необходимости усиливать муколитический эффект препаратами одной лекарственной группы. Более того, это можно считать врачебной ошибкой, т.к. у ребенка с ОРИ можно вызвать чрезмерное отделение мокроты, которое малыш не сможет эффективно эвакуировать и возможно возникновение осложнений в виде «синдрома заболачивания легких», обструкции с дыхательной недостаточностью и даже пневмонии. При лечении больных хроническими бронхитами, например, на фоне муковисцидоза или тяжелых врожденных пороков развития бронхов с выраженным мукостазом, такая практика, наоборот, успешно применяется. Используя различные свойства активных молекул, можно создавать наиболее эффективные сочетания муколитиков, а также применять различные пути их введения (например, чередовать ингаляции с приемом внутрь) [31].
Следует отметить, что ацетилцистеин рекомендован Стандартами первичной медико-санитарной помощи при ОРИ и синуситах; ацетилцистеин и амброксол включены в стандарты амбулаторно-поликлинической помощи при остром бронхите. Указанные нормативные документы дают возможность практическому врачу обоснованно использовать эти лекарственные средства [32].
Таким образом, к основным практическим выводам и рекомендациям подбора терапии ОРИ для детей можно отнести следующие:
- при неосложненных ОРИ у детей в равной степени можно применять с муколитической целью и ацетилцистеин и амброксол, обладающие одинаковой доказанной эффективностью и имеющие высокий уровень безопасности. Следует учитывать, что ацетилцистеин будет действовать несколько быстрее, т.к. является прямым муколитиком, но не «сильнее»;
- при острой инфекции, которая протекает с явлениями бронхита и риносинусита, целесообразно применять ацетилцистеин, который будет разжижать не только бронхиальный, но и назальный секрет, а также уменьшать воспаление в околоносовых пазухах. Детям старше двух лет может быть рекомендован АЦЦ® (ацетилцистеин 20 мг/мл) в удобной для детей форме – сиропа без сахара, спирта и красителей;
- если ОРИ протекает помимо кашля с выраженными симптомами интоксикации (высокой температурой, резкой слабостью), следует выбирать ацетилцистеин, не только благодаря его муколитическим, но и антиоксидантным и противовоспалительным свойствам, которые будут нивелировать эти симптомы;
- при затяжном или хроническом воспалении в дыхательных путях целесообразно применять амброксол, используя его свойство стимулировать синтез сурфактанта, который снижается при длительном бронхите;
- в случае наличия показаний к назначению антибиотиков предпочтительна комбинация с ацетилцистеином, который обладает свойством разрушать биопленки бактерий и таким образом может усиливать действие антибиотика;
- для детей младше двух лет препаратом выбора остается амброксол (любые лекарственные формы, в т.ч. растворы для ингаляций, но необходимо помнить о дренаже);
- возможно комбинировать пути ведения муколитика в зависимости от ситуации: ½ суточной дозы назначить в виде небулайзерной ингаляции, а ½ – суточной дозы внутрь.